삼성바이오에피스의 바이오시밀러 ‘렌플렉시스’가 미국 진출의 포문을 열었다.
삼성바이오에피스는 21일(현지시간) 미국 FDA(식품의약국)로부터 자가면역질환 치료제 렌플렉시스(SB2, 성분명: 인플릭시맙)에 대한 판매 허가 승인을 받았다고 밝혔다.
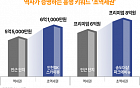
렌플렉시스는 작년 기준 연간 9조3000억 원 이상 팔리는 존슨앤존슨의 항체의약품 ‘레미케이드’(성분명: 인플릭시맙)의 바이오시밀러다. 류머티스 관절염, 궤양성 대장염, 크론병, 강직성 척추염, 건선성 관절염과 건선에 적응증을 가지고 있다.
이번 승인은 한국(2015년), 유럽, 호주(이상 2016년)에 이어 렌플렉시스(유럽명: 플릭사비)의 네 번째 판매 허가 승인이다. 삼성바이오에피스는 작년 3월 FDA에 렌플렉시스 판매 허가 신청을 하고 13개월만에 허가 승인을 받았다. 파트너사인 글로벌 제약사 머크가 미국에서의 판매를 담당할 예정이다. 현지 판매는 이르면 6개월 후부터 가능하다.
삼성바이오에피스 관계자는 “연구개발(R&D) 역량과 제품이 국제적으로 인정받는 계기가 됐다”며 “또 세계 최대 바이오 의약품 시장인 미국에서 글로벌 제약사들과 당당히 경쟁할 수 있는 초석을 마련했다”고 밝혔다.
삼성바이오에피스는 지난해 3월 미국 FDA에 렌플렉시스 판매 허가 신청을 하고 13개월만에 허가 승인을 받았으며 파트너사인 글로벌 제약사 Merck社가 미국에서의 판매를 담당할 예정이다.
한편 삼성바이오에피스는 현재 엔브렐 바이오시밀러(SB4, 성분명: 에타너셉트)인 ‘브렌시스’를 호주, 캐나다, 한국, 유럽(유럽명: 베네팔리)등에 판매 중에 있다. 또 휴미라 바이오시밀러(SB5, 성분명: 아달리무맙), 허셉틴 바이오시밀러(SB3, 성분명: 트라스투주맙)는 EMA(유럽의약품청)에서 판매 허가 심사 중에 있다.

![용리단길부터 예산시장까지…백종원도 경고 날린 '핫플레이스'의 이면 [이슈크래커]](https://img.etoday.co.kr/crop/140/88/2104730.jpg)
![10% '껑충'…올해 김장값 얼마? [데이터클립]](https://img.etoday.co.kr/crop/140/88/2104829.jpg)
![‘13월의 보너스’ 연말정산 세액공제, 더 받기 위해 알아야 할 것들은? [경제한줌]](https://img.etoday.co.kr/crop/140/88/2104687.jpg)
![한동훈 또다시 침묵...불붙은 與 당원게시판 싸움 점입가경 [종합]](https://img.etoday.co.kr/crop/140/88/2098740.jpg)






!["12월까지 미국보다 좋은 장세 가능" 국내 증시 반격 '여기'서 시작됩니다 ㅣ 염승환 이사 [찐코노미]](https://i.ytimg.com/vi/Q_TIlN-sGWw/mqdefault.jpg)










![[찐코노미] "12월까지 미국보다 좋을 것"…국내 증시 반격 '여기'서 시작된다?](https://img.etoday.co.kr/crop/300/170/2104841.jpg)
![킨텍스서 열린 2024 스마트건설 엑스포 [포토]](https://img.etoday.co.kr/crop/300/190/2104778.jpg)