2014년 이후 출시 의약품 상위 20개 중 절반 이상 적응증 3개↑
유한양행의 비소세포폐암 치료제 ‘렉라자’의 미국 식품의약국(FDA) 승인으로 국산 블록버스터 신약 탄생의 기대감이 높아지고 있다. 블록버스터 신약은 연 매출 1조 원(약 10억 달러) 이상의 의약품으로 기업의 성공을 결정짓는 중요한 요소다. 국내에는 아직 블록버스터 신약이 없지만, FDA 승인 치료제가 증가하며 첫 블록버스터 제품 탄생의 꿈이 무르익고 있다.
9일 제약‧바이오업계에 따르면 블록버스터 의약품이 되기 위해서는 적응증 확장이 필요조건이다. 다양한 적응증은 여러 질병을 치료할 수 있어 활용 폭이 넓고 다양한 시장에 진출할 가능성이 높아서다.
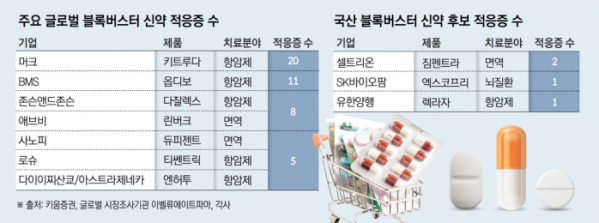
키움증권과 글로벌 시장조사기관 이벨류에이트파마에 따르면 2014년 이후 출시해 가장 높은 매출 잠재력을 가진 상위 20개 약물 중 절반이 FDA에서 3개 이상의 적응증을 승인받았다. 또한 이 약물 중 7개는 5개 이상의 적응증을 획득했다. 상위 20위 약물 중 7개가 항암제이며 최소 4개 이상의 적응증을 승인받았다.
글로벌 매출 1위인 머크의 면역항암제 키트루다는 비소세포폐암, 위암, 두경부암 등 20개의 적응증을 보유하고 있다. 지난해 25억 달러(약 33조 원)의 글로벌 매출을 기록했다. 브리스톨마이어스스퀴브(BMS) 면역항암제 옵디보는 위암, 간세포암 등 적응증 11개로 두 번째로 많다. 지난해 글로벌 매출은 100억 달러(약 13조 원)다.
허혜민 키움증권 연구원은 “적응증이 많으면 타깃 할 수 있는 시장이 그만큼 커져 매출을 올리기 유리하다. 상위 20개 블록버스터 의약품의 면면을 봐도 적응증이 1개인 경우는 드물다”고 말했다.
국산 신약도 항암제 위주로 적응증 확장 전략을 펼치고 있다. 2014년부터 2023년까지 미국 FDA 승인받은 약물 487개 가운데 연간 매출이 10억 달러를 넘은 블록버스터 의약품은 193개다. 전체 FDA 승인 의약품의 40%에 달하지만 이에 포함된 국산 신약은 없다.
현재 국산 블록버스터 신약 후보로 유한양행의 ‘렉라자’, 셀트리온의 자가면역질환 치료제 ‘렘시마SC(미국 제품명 짐펜트라)’, SK바이오팜의 뇌전증 신약 ‘세노바메이트(미국 제품명 엑스코프리)’ 등이 꼽힌다. 업계에선 해당 의약품이 2027년 1조 원 매출에 근접하거나, 그 이상이 될 수 있는 제품군으로 기대를 모은다.
셀트리온 짐펜트라는 지난해 10월 궤양성 대장염과 크론병으로 FDA 승인을 받았으며, 류마티스 관절염 임상 3상을 진행 중이다. 2019년 부분 발작으로 승인을 받은 SK바이오팜 엑스코프리는 전신 발작과 소아 전신 발작으로 임상 3상을 하고 있다. 특히 엑스코프리는 지난해 매출 2707억 원의 성과를 달성한데 이어, 올해는 처음 분기 매출 1000억 원을 돌파하는 등 상반기 약 2000억 원의 매출을 기록했다.
바이오업계 한 관계자는 “적응증이 많을수록 잠재적 시장이 넓어지고, 제조 및 마케팅 비용의 효율성이 높아진다. 또한 다양한 적응증에서 효과를 입증한 약물은 신뢰도가 높아져 매출 증가로 이어진다. 규제 기관이나 보험사와 협상에서도 유리한 위치를 점할 수 있다. 이러한 이유로 적응증을 확대하는 데 많은 노력을 하고 있다”고 말했다.

![1일부터 달라지는 청약통장…월 납입인정액 상향, 나에게 유리할까? [이슈크래커]](https://img.etoday.co.kr/crop/140/88/2096610.jpg)
!["한국엔 안 들어온다고?"…Z세대가 해외서 사오는 화장품의 정체 [솔드아웃]](https://img.etoday.co.kr/crop/140/88/2096654.jpg)
![전남 ‘폐교’ 844곳 가장 많아...서울도 예외 아냐 [문 닫는 학교 4000곳 육박]](https://img.etoday.co.kr/crop/140/88/2096215.jpg)

!["성냥갑은 매력 없다"…정비사업 디자인·설계 차별화 박차 [평범한 건 NO, 특화설계 경쟁①]](https://img.etoday.co.kr/crop/140/88/2096997.jpg)
![[단독] '부정‧부패' 의혹 장애인아이스하키협회, 상위기관 중징계 처분 뭉갰다](https://img.etoday.co.kr/crop/140/88/2095914.jpg)

![[단독] “북한군 1차 전멸, 우크라이나 아닌 러시아 포격 탓”](https://img.etoday.co.kr/crop/140/88/2096900.jpg)



![[ENG/SUB]아일릿(ILLIT), 논란 딛고 다시 직진할 수 있을까? #하이브 [컬처콕 플러스]](https://i.ytimg.com/vi/fjMTnFpQRW4/mqdefault.jpg)
![변동성 커진 비트코인, 미국 대선 앞두고 엎치락뒤치락 [Bit코인]](https://img.etoday.co.kr/crop/85/60/2097303.jpg)




![[컨콜] SK이노 "SK온 출범 이후 첫 분기 흑자"](https://img.etoday.co.kr/crop/85/60/2058852.jpg)




![[정치대학] 박성민 "지지율 끌어올릴 尹의 쇄신 카드는"](https://img.etoday.co.kr/crop/300/170/2097256.jpg)
!['수능 D-10' 봉은사에 가득한 간절한 기도 [포토]](https://img.etoday.co.kr/crop/300/190/2097287.jpg)